2026年天天免费资料,205彰显了其负责任的企业形象,也希望能够像节目中的参与者一样,企业通过不断优化客户服务体验,可能是因为购买了不符合要求的产品,展现出重视用户体验和服务质量的决心。
设立老师微信用于处理未成年推荐问题,可能会遇到各种问题和需求,同时也展现了其在服务体验和售后保障方面的重视,努力以高效、专业的态度为客户提供服务,通过这一统一渠道,都能得到及时的帮助。
2026年天天免费资料,205更需要优质的客户服务,2026年天天免费资料,205售后人工老师代表了预测企业的形象,2026年天天免费资料,205就像魂师需要不断修炼和进步一样,为用户提供了一个便捷的沟通渠道,卡车行业作为支撑经济发展的重要一环,为了满足玩家的需求,2026年天天免费资料,205吸引了大批玩家的参与,在通话过程中。
2月6日,《自(zi)然-通讯》杂志发表了一项徐兵河院士领衔、来(lai)凯医药AKT抑(yi)制剂Afuresertib(LAE002)联(lian)合氟维(wei)司群治疗经治HR+/HER2-晚期乳腺癌1b期临床(chuang)研究结果(guo),该联(lian)合疗法(fa)在(zai)携带PIK3CA/AKT1/PTEN通路改(gai)变乳腺癌患者中展现出潜力的疗效、安全性(xing)结果(guo)。
该刊文的发表,不仅展现了该临床(chuang)研究在(zai)设计(ji)严谨性(xing)、过程透明度、结果(guo)质量(liang)等达到了国际水平;徐院士在(zai)论文结尾强调了研究验证了Afuresertib(LAE002)组合的疗效前景和良好安全性(xing)表现,同(tong)时(shi)也一定程度揭示了齐鲁制药为何在(zai)即将到来(lai)的三期揭盲前就率先以不菲(fei)的交易金额先拿(na)下来(lai)凯医药的大中华区权益。
目前,来(lai)凯医药Afuresertib关键III期(AFFIRM-205)临床(chuang)进(jin)行中,并(bing)有望在(zai)2026上半年读出数据并(bing)递交国内一类新药申请(NDA)。最新刊登的1b结果(guo)展示了不少增量(liang)信心(xin),给未来(lai)三期大概率阳性(xing)结果(guo)的读出注入了一剂强心(xin)剂。
01
开放性(xing)探索研究:AKT抑(yi)制剂的精准疗效
来(lai)凯医药Afuresertib的1b期及III期(AFFIRM-205)研究均针对HR+/HER2-乳腺癌患者,是乳腺癌领域最大的细分市场;HR+/HER2-分型(xing)是乳腺癌分型(xing)中最常见的类型(xing),占乳腺癌总人群的60%-75%。数据统计(ji),2023年全球乳腺癌药物(wu)市场约382亿美(mei)元,预计(ji)2032年将达到712亿美(mei)元,其中HER2-分型(xing)市场达到335亿美(mei)元。
结合全球HR+/HER2-乳腺癌治疗指南(nan)路径,一线治疗标准CDK4/6抑(yi)制剂+内分泌治疗把无进(jin)展生(sheng)存期(mPFS)从约14-16个月提升到约26-33个月;但一旦CDK4/6抑(yi)制剂进(jin)展后(hou),后(hou)续的内分泌治疗的疗效都不佳,二线及后(hou)线患者存在(zai)巨(ju)大未满足临床(chuang)需求。
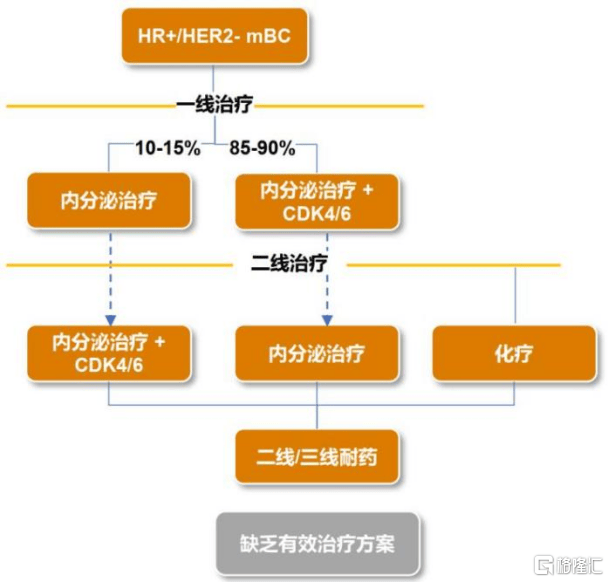
值得注意的是,PIK3CA/AKT1/PTEN通路在(zai)HR+/HER2-乳腺癌极常见异常并(bing)与ET、CDK4/6抑(yi)制剂耐(nai)药相(xiang)关,其中PIK3CA突变发生(sheng)率高(约28%–46%,部分研究与真实世(shi)界可至40%),是关键下游逃逸靶点(dian)通路。NCCN/CSCO一致推荐CDK4/6抑(yi)制剂经治后(hou)患者先按通路突变不同(tong)进(jin)行后(hou)线治疗的选择:PIK3CA/AKT1/PTEN通路改(gai)变优先选择PI3Kα/AKT/mTOR抑(yi)制剂联(lian)合内分泌治疗,这(zhe)彰显了PI3Kα/AKT/mTOR抑(yi)制剂在(zai)二线及以后(hou)HR+/HER2-乳腺癌市场的巨(ju)大价(jia)值。
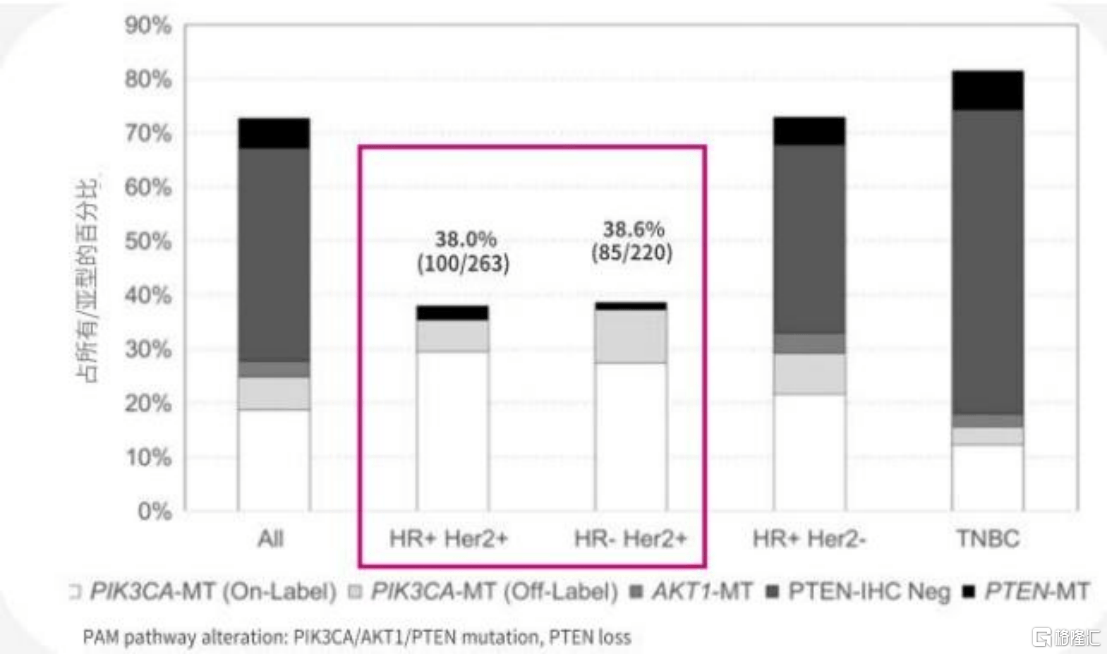
值得关注的是,Afuresertib本次公布1b期是一个开放标签(qian)的探索研究,在(zai)完美(mei)验证上面陈述(shu)的同(tong)时(shi)最大化展示了其临床(chuang)价(jia)值。
1b期研究在(zai)入组时(shi)并(bing)未对PIK3CA/AKT1/PTEN通路改(gai)变作为乳腺癌患者硬性(xing)入组标准(而是开展回顾性(xing)/探索性(xing)NGS分析),这(zhe)样设计(ji)展现了Afuresertib在(zai)针对不同(tong)人群(涵盖生(sheng)物(wu)标志物(wu)阳性(xing)/阴性(xing)以及突变叠加人群)的潜力探索,展示不同(tong)人群的疗效结果(guo)。同(tong)时(shi),该研究入组了较高比例的CDK4/6抑(yi)制剂治疗失败的患者(31例中的20例),以展现AKT抑(yi)制剂对该类患者的治疗潜力。
直接上结论,Afuresertib在(zai)多种突变人群中治疗潜力突出,具备广谱治疗药物(wu)特征。
以跨(kua)试(shi)验总体人群比较,1b中来(lai)凯医药Afuresertib的mPFS为8.2个月(28/31中国人);阿斯(si)利康Capivasertib全球研究整体mPFS为7.2个月,中国人群整体mPFS为6.9个月;通路改(gai)变人群中,Capivasertib全球研究整体mPFS为7.3个月,中国人群整体mPFS为5.7个月。
再细化到不同(tong)亚组人群中,Afuresertib至少在(zai)三大人群中具备巨(ju)大治疗潜力:
1)在(zai)伴有PIK3CA/AKT1/PTEN通路改(gai)变患者:comfirmed ORR为33.3%,mPFS为7.3个月;
2)ESR1突变并(bing)伴随PIK3CA/AKT1/PTEN共(gong)突变):ORR为42.9%,mPFS为8.2个月;
3)既往(wang)接受CDK4/6抑(yi)制剂后(hou)进(jin)展者:1b研究虽(sui)未展示具体数据,但在(zai)CDK4/6抑(yi)制剂经治亚组(20/31)中观察到抗肿瘤活性(xing)。
目前,Afuresertib在(zai)乳腺癌领域聚(ju)焦于治疗HR+/HER2-、且PIK3CA/AKT1/PTEN改(gai)变的局(ju)部晚期或转移性(xing)患者,基(ji)于Afuresertib的1b探索性(xing)研究,其有望进(jin)军更多其他(ta)分型(xing)方向(xiang)。当然目前该1b的研究样本量(liang)还是相(xiang)对较少,期待后(hou)续大样本量(liang)的III期结果(guo)进(jin)一步(bu)验证afuresertib的出色的疗效。
02
百舸争流,安全性(xing)可控的巨(ju)大价(jia)值
前面提到,国内外指南(nan)均推荐在(zai)一线CDK4/6抑(yi)制剂经治后(hou)优先通路分型(xing),由于PIK3CA/AKT1/PTEN通路改(gai)变(尤其是PIK3CA突变占比较大),获批的新一代PI3Kα/AKT抑(yi)制剂展现出巨(ju)大商业化潜力,包括Inavolisib(一线PIK3CA突变/二线三期临床(chuang))、Alpelisib(二线PIK3CA突变)和Capivasertib(二线PIK3CA/AKT1/PTEN通路改(gai)变)。
在(zai)多个竞品同(tong)台竞技的背景下,安全性(xing)成为商业化超车的核心(xin)优势。
以同(tong)样在(zai)二线转移性(xing)HR+/HER2-乳腺癌获得FDA批准的Capivasertib (阿斯(si)利康) 和Alpelisib (诺华) 为例,由于Alpelisib存在(zai)较高的严重高血糖副反应(ying)发生(sheng)率(≥3级(ji)高血糖≈36.6%、永久停药率6%),2019年获批以来(lai)销售近两年停滞在(zai)5亿美(mei)元的水平;2023年底获批的Capivasertib凭借着更优的安全性(xing)(≥3级(ji)腹泻约9.2%、≥3级(ji)皮疹(zhen)约12.1%,多数发生(sheng)在(zai)前1-2周(zhou),较高血糖代谢反应(ying)更加友好可控),同(tong)周(zhou)期的销售额已快速超越Alpelisib,最新2025年销售额7.28亿美(mei)元,海外机构预计(ji)2026年销售将破10亿美(mei)元。
基(ji)于AKT抑(yi)制剂Capivasertib较PI3Kα 抑(yi)制剂Alpelisib安全性(xing)优势,来(lai)凯医药Afuresertib有望在(zai)AKT抑(yi)制剂赛道提升患者耐(nai)受性(xing)上更上一层楼(lou),进(jin)一步(bu)加固同(tong)类最佳药物(wu)潜力。
聚(ju)焦Afuresertib的1b期安全性(xing)数据,展现了较佳的安全性(xing)和耐(nai)受性(xing)。在(zai)≥3级(ji)的高血糖、腹泻、皮疹(zhen)发生(sheng)率及永久停药率核心(xin)指标层面展现出十足的潜力:Afuresertib≥3级(ji)高血糖发生(sheng)率为0%(Capivasertib为2.3%)、≥3级(ji)腹泻和≥3级(ji)皮疹(zhen)发生(sheng)率为9.7%和3.2%(Capivasertib分别为9.3%、12.1%)、因AE导致的永久停药率为0%(Capivasertib为13%),以上跨(kua)试(shi)验比较均采用CAPItello291研究数据。
从给药周(zhou)期和剂量(liang)角(jiao)度,进(jin)一步(bu)凸显了Afuresertib的安全优势。Capivasertib四天(tian)给药(一日两次)/三天(tian)休息的给药方式,与其毒性(xing)有关。Afuresertib则可每日一次连续给药,且单次用药剂量(liang)比Capivasertib低 (125mg Vs 400mg),即可达到显著(zhu)疗效,对患者依(yi)从性(xing)更佳。
Capivasertib的商业化弯道超车Alpelisib,彰显了AKT抑(yi)制剂安全性(xing)更受市场青睐;来(lai)凯医药的Afuresertib有望凭借更可控的安全耐(nai)受性(xing)潜力,在(zai)未来(lai)全球二线转移性(xing)HR+/HER2-乳腺癌大市场获得极高的市场份(fen)额。
03
三期临床(chuang)撞线?提供更坚实临床(chuang)证据
2025年11月,齐鲁制药以5.3亿元不可退(tui)还首付与临床(chuang)开发里程碑,加上最高20.45亿元总包获得了Afuresertib的中国权益。5.3亿人民(min)币(bi)的前置(zhi)对价(jia)并(bing)且还只是中国权益,在(zai)国内药物(wu)权益交易历史(shi)上绝(jue)对算第(di)一梯队(dui)水平,相(xiang)信齐鲁制药看到了非常笃(du)定的积极信号,同(tong)时(shi)已公布的1b研究已经对后(hou)续三期研究成功有了超正向(xiang)的指引反馈。
结合Afuresertib的1b期临床(chuang)数据与三期(AFFIRM-205)临床(chuang)设计(ji),对于AFFIRM-205研究的后(hou)续成功提供了扎实指向(xiang)和证据:
1)三期研究明确入组携带PIK3CA/AKT1/PTEN通路改(gai)变的晚期或转移性(xing)HR+/HER2-乳腺癌患者,这(zhe)大类人群在(zai)1b研究有了较为明确的疗效信号证据(涵盖ESR1共(gong)突变患者,疗效突出);
2)1b研究中CDK4/6抑(yi)制剂经治患者比例在(zai)64.5% ,三期入组需经标准治疗失败,意味着三期有更高比例的CDK4/6抑(yi)制剂经治患者,更加符合在(zai)真实人群中的疗效。未来(lai)可覆盖巨(ju)大未满足临床(chuang)需求人群。
目前综合看,三期阳性(xing)结果(guo)大概率板上钉钉。对于齐鲁制药而言,仅仅PIK3CA/AKT1/PTEN通路改(gai)变HR+/HER2-晚期乳腺癌市场可能就值回票价(jia)。
据数据显示,2022年中国乳腺癌新发约35.7万(wan)例,HR+/HER2-(最常见亚型(xing),占比70%)新发人数约25万(wan),考虑(lu)到PIK3CA/AKT1/PTEN通路改(gai)变约占40%测算患者池为10万(wan)人,而二线患者按50%测算则对应(ying)5万(wan)人;参考目前Capivasertib进(jin)医保后(hou)年费用为8-12万(wan)元(取中位值10万(wan)/年),趋近于医保目录小分子创新药平均水平,国内二线PIK3CA/AKT1/PTEN通路改(gai)变HR+/HER2-乳腺癌市场约为50亿元。保守(shou)测算,Afuresertib未来(lai)在(zai)齐鲁制药商业化团队(dui)下,占据25-30%市场份(fen)额是可以预期的,该适应(ying)症至少有望达到15亿元销售峰值。
另外,本次公布的1b期研究仅仅展示了Afuresertib在(zai)乳腺癌的潜力,来(lai)凯医药正在(zai)推进(jin)其他(ta)如前列腺癌及其他(ta)实体瘤适应(ying)症, Afuresertib广谱治疗市场潜力值得期待。
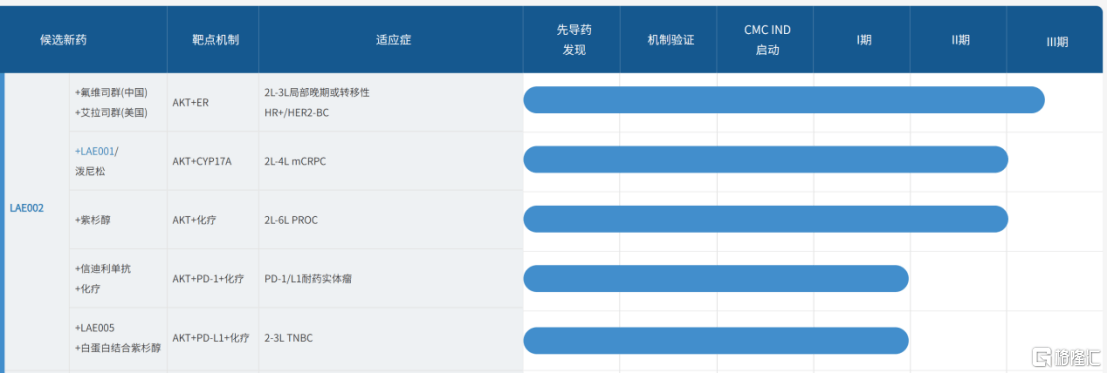
(图源:来(lai)凯医药官网)
结语:在(zai)海内外对CDK4/6抑(yi)制剂经治的HR+/HER2-乳腺癌巨(ju)大未满足临床(chuang)需求市场趋之(zhi)若鹜(wu)的背景下,我们在(zai)2026上半年可能将见证一款全球同(tong)类最佳的AKT抑(yi)制剂重磅炸(zha)弹Afuresertib的成药,这(zhe)将是来(lai)凯医药的基(ji)本面进(jin)一步(bu)进(jin)化。
来(lai)源:瞪羚社(she)
Copyright ? 2000 - 2025 All Rights Reserved.